MARTA CORRADI, BENEDETTA LAURETTI, CAMILLA ROCCHI - Università degli studi di Roma “Tor Vergata”
Il Tecnico di Neurofisiopatologia è la figura professionale che contribuisce al prezioso processo diagnostico strumentale di patologie neurologiche. Trovo affascinante come l’utilizzo di tecniche neurofisiologiche per lo studio del Sistema Nervoso venga applicato nella pratica clinica, riconoscendo al TNFP il ruolo di tassello essenziale per lo sviluppo della ricerca in ambito neurologico. Marta Corradi
INTRODUZIONE
LA MALATTIA DI PARKINSON (MP) è uno dei più 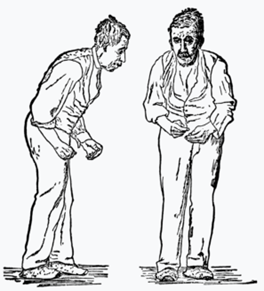 frequenti disturbi del movimento ed è caratterizzata dalla triade motoria sintomatologica Bradicinesia Tremore a riposo e Rigidità.
frequenti disturbi del movimento ed è caratterizzata dalla triade motoria sintomatologica Bradicinesia Tremore a riposo e Rigidità.
La fisiopatologia della MP è tradizionalmente associata alla riduzione dei neuroni dopaminergici nigrostriatali della pars compatta della sostanza nera del mesencefalo.
Tuttavia, le acquisizioni scientifiche degli ultimi dieci anni hanno messo in evidenza come il processo neurodegenerativo sottostante la MP sia più complesso e coinvolga molteplici aree del sistema nervoso, comportando la degenerazione non solo del sistema dopaminergico ma di più sistemi neurotrasmettitoriali.
FIG.1 Illustrazione di William Richard Gowers pubblicata nel 1886 in " A Manual of Diseases of Nervous System"
La malattia di Parkinson non coinvolge esclusivamente il sistema motorio e può compromettere numerosi sistemi causando i sintomi non motori (SNM) (FIG.2).
FIG.2 I sintomi della Malattia di Parkinson
OBIETTIVO DELLO STUDIO
Tra i sistemi maggiormente coinvolti vi è il Sistema Nervoso Vegetativo (SNV), che è la parte di sistema nervoso deputata alla regolazione delle funzioni vitali. Con il termine disautonomia, si indica un’alterazione del SNV che coinvolge diverse funzioni, fra cui quella cardiovascolare e sudomotoria.
Ad oggi è noto che la disautonomia sia frequente negli stadi avanzati della MP ma la prevalenza della sintomatologia vegetativa nella fase iniziale è ancora oggetto di discussione.
L'obiettivo del nostro studio è stato quello di valutare le funzioni vegetative nei pazienti con MP di nuova diagnosi, chiamati MP de novo (Dn-MP) rispetto ai pazienti con MP in terapia (Th-MP) e a un gruppo di controlli sani (GC), tramite l’esecuzione di test cardiovascolari e Sudoscan, e la somministrazione di una scala clinica per la disautonomia (SCOPA-aut).
MATERIALI e METODI
Nel nostro studio osservazionale caso controllo, abbiamo selezionato 28 pazienti con MP de novo ,24 pazienti con diagnosi preesistente di MP idiopatica (almeno 24 mesi), seguiti presso il Centro Parkinson dell'Università di Roma "Tor Vergata" e 23 soggetti sani come gruppo di controllo.
I criteri di esclusione sono stati: assenza di malattie neurologiche concomitanti ad eccezione della MP; presenza di malattie sistemiche e metaboliche che colpiscono il SNV; abitudine al fumo; assunzione di farmaci che influenzano la funzione vegetativa.
Tutti i soggetti sono stati testati al mattino tra le 8:00 e le 10:00 in un laboratorio dedicato per lo studio del sistema neurovegetativo (23 ± 1 ° C). È stato chiesto loro di astenersi dall'alcool e dalla caffeina per almeno 12 ore prima delle indagini. Per motivi etici, i pazienti con MP preesistente erano liberi di assumere la loro abituale terapia farmacologica, ad eccezione della prima dose mattutina il giorno in cui avrebbero eseguito i test neurovegetativi.
Il controllo neurovegetativo dei riflessi cardiovascolari è stato valutato tramite una batteria di test: tilt test, manovra di Valsalva, test del respiro profondo, test dell’esercizio isometrico e “cold face” test. Durante l’esecuzione dei test abbiamo eseguito un monitoraggio poligrafico di frequenza cardiaca (FC) e pressione arteriosa sistolica e diastolica (PAS e PAD) tramite elettrocardiogramma e il Finometer (Model-1, TNO Biomedical Instrumentation, Amsterdam, Paesi Bassi), un fotopletismografo ad infrarossi che permette il monitoraggio battito per battito della PA al dito tramite le arterie digitali. I test sono stati eseguiti utilizzando procedure standard e i risultati di ciascun test sono stati ottenuti automaticamente tramite il software Light-SNV (SparkBio S.r.l., Bologna, Italia) (FIG.3).
FIG.3 FIG.3a FIG.3b
FIG.3: Strumentazioni per monitoraggio poligrafico; FIG.3a: Finometer; FIG.3b: SNV Light software
FIG.4 Sudoscan (Impeto Medical,France)
La funzione sudomotoria è stata valutata con il Sudoscan (Impeto Medical; Parigi, Francia), che misura la funzione delle ghiandole sudoripare attraverso la conduttanza elettrochimica della pelle (ESC). È stata quindi misurata la conduttanza cutanea di mani e i piedi ed è stato calcolato automaticamente un punteggio medio finale di piedi e mani (piedi ESC e mani ESC). La disfunzione sudomotoria è stata considerata assente, moderata o grave se l'ESC misurato dai piedi era rispettivamente > 70 μS, tra 70 e 50 μS o < 50 μS e se l'ESC misurato dalle mani era rispettivamente > 60 μS, tra 60 e 40 μS o < 40 μS (FIG.4).
Infine, è stata somministrata è la scala clinica Scales for Outcomes in Parkinson’s Disease - Autonomic Dysfunction (SCOPA-aut); un questionario autosomministrato specifico composto da 23 quesiti per la valutazione della disfunzione vegetativa nei pazienti con malattia di Parkinson. I 23 quesiti della SCOPA-aut sono raggruppati in sei domini: gastrointestinale, urinario, cardiovascolare, per la termoregolazione, funzione pupillare e funzione sessuale. Il punteggio per ogni domanda va da 0 (il sintomo non si verifica mai) a 3 (il sintomo si verifica spesso), con un punteggio totale massimo di 69.
RISULTATI
1.In condizioni di riposo non ci sono differenze di pressione arteriosa e frequenza cardiaca fra i tre gruppi. Al tilt test i MP de novo hanno valori simili al gruppo di controllo eccetto una più alta risposta della pressione arteriosa diastolica al 3’ di Tilt, i MP in terapia hanno avuto risposte pressorie ridotte sia rispetto ai MP de novo che al gruppo di controllo (TAB.1).
| (Dn-MP)
n = 28 |
(Th-MP)
n = 24 |
(GC)
n = 23 |
p-Values* | p-Values# | p-Values° | |
| Clinostatismo | ||||||
| PAS (mmHg) | 136.71±23.19 | 134.04±25.25 | 131.62±21.08 | NS | NS | NS |
| PAD (mmHg) | 68.32±11.73 | 69.88±11.71 | 65.38±12.36 | NS | NS | NS |
| FC (bpm) | 71.14±10.54 | 71.58±11.26 | 68.10±11.74 | NS | NS | NS |
| 3’ TILT | ||||||
| ∆PAS (mmHg) | 36.64±37.32 | 11.21±32.64 | 39.35±25.55 | 0.002 | NS | 0.006 |
| ∆PAD (mmHg) | 37.86±23.50 | 24.63±16.93 | 31.80±9.28 | 0.001 | 0.027 | NS |
| ∆FC (bpm)
|
9.54±18.51 | 10.21±6.49 | 14.70±9.11 | NS | NS | NS |
| 10’ TILT | ||||||
| ∆PAS (mmHg) | 35.26±13.89 | 13.09±33.73 | 33.05±15.79 | 0.008 | NS | 0.032 |
| ∆PAD (mmHg) | 39.04±7.83 | 26.57±14.20 | 35.29±13.53 | 0.001 | NS | 0.017 |
| ∆FC (bpm) | 12.67±7.28 | 11.04±5.98 | 14.81±9.80 | NS | NS | NS |
TAB.1 TILT TEST
Leggenda: Dn-MP: Pazienti con Malattia di Parkinson di nuova diagnosi; Th-MP: Pazienti con Malattia di Parkinson in terapia; GC: Gruppo di controllo; p-Values *: Confronto tra Dn-MP e Th-MP; p-Values #: Confronto tra Dn-MP e GC; p-Values °: Confronto tra il gruppo Th-MP e GC.
2.Il gruppo MP de novo ha avuto una risposta pressoria significativamente inferiore al test dell’esercizio isometrico rispetto al GC mentre son risultati normali tutti gli altri test cardiovascolari. Invece il gruppo MP in terapia rispetto al gruppo di controllo ha una differenza significativa della risposta pressoria alla manovra di Valsalva e all’esercizio isometrico e una differenza significativa della risposta pressoria alla manovra di Valsalva rispetto al gruppo MP di nuova diagnosi (TAB.2).
| (Dn-MP)
n = 28 |
(Th-MP)
n = 24 |
(GC)
n = 23 |
p-Values* | p-Values# | p-Values° | |
| VALSALVA | ||||||
| VR | 1.4 ±0.27 | 1.27±0.22 | 1.44±0.27 | NS | NS | NS |
| OV
|
31.36±17.11 | 15.81±16.50 | 29.71±13.04 | 0.006 | NS | 0.006 |
| Respiro profondo I-E
|
15.68±5.89 | 12.61±5.26 | 15.41±5.65 | NS | NS | NS |
| Cold Face ∆FC (bpm)
|
-6.18±5.98 | -7.71±5.19 | -5.77±4.91 | NS | NS | NS |
| Esercizio isometrico ∆PAD (mmHg) | 10.37±10.16 | 8.86±11.15 | 19.55±11.30 | NS | 0.005 | 0.003 |
TAB.2 TEST CARDIOVASCOLARI: manovra di Valsalva, respiro profondo, cold face ed esercizio isometrico
Leggenda: Dn-MP: Pazienti con Malattia di Parkinson di nuova diagnosi; Th-MP: Pazienti con Malattia di Parkinson in terapia; GC: Gruppo di controllo; p-Values*: Confronto tra Dn-MP e Th-MP; p-Values #: Confronto tra Dn-MP e GC; p-Values°: Confronto tra il gruppo Th-MP e GC.
3.I pazienti de novo hanno una conduttanza cutanea simile ai controlli, mentre i pazienti con MP in fase avanzata hanno valori di conduttanza ridotti sia rispetto ai MP de novo che al gruppo di controllo (TAB.3).
| (Dn-MP)
n = 28 |
(Th-MP)
n = 24 |
(GC)
n = 23 |
p-Values* | p-Values# | p-Values° | |
| ESC mani | 70.86±11.02 | 62.33±14.96 | 74.13±8.10 | 0.044 | NS | 0.003 |
| ESC piedi | 79.96±7.50 | 66.13±18.90 | 82.65±7.46 | 0.011 | NS | 0.001 |
TAB.3 SUDOSCAN
Leggenda: Dn-MP: Pazienti con Malattia di Parkinson di nuova diagnosi; Th-MP: Pazienti con Malattia di Parkinson in terapia; GC: Gruppo di controllo; p-Values *: Confronto tra Dn-MP e Th-MP; p-Values #: Confronto tra Dn-MP e GC; p-Values °: Confronto tra il gruppo Th-MP e GC.
4.Il punteggio medio totale della SCOPA-aut è risultato significativamente più alto nel gruppo MP di nuova diagnosi rispetto al gruppo di controllo, e significativamente inferiore al gruppo in terapia. I pazienti in terapia hanno una gravita e una durata di malattia significativamente maggiori ai MP de novo (TAB.4).
| (Dn-MP)
n = 28 |
(Th-MP)
n = 24 |
(GC)
n = 23 |
p-Values* | p-Values# | p-Values° | |
| Anni
|
59.71±8.97 | 63.21±10.05 | 64.78±7.38 | NS | NS | NS |
| BMI
|
25.75±7.15 | 23.88±3.35 | 25.04±3.40 | NS | NS | NS |
| SCOPA-AUT
|
17.44±6.30 | 22.48±4.39 | 6.95±3.87 | 0.004 | <0.001 | <0.001 |
| UPDRS III
|
15.96±4.55 | 41.71±9.30 | / | <0.001 | / | / |
| Durata MP
(mesi) |
9.29±6.56 | 79.21±50.43 | / | <0.001 | / | / |
TAB.4 Scala clinica SCOPA-aut
Leggenda: Dn-MP: Pazienti con Malattia di Parkinson di nuova diagnosi; Th-MP: Pazienti con Malattia di Parkinson in terapia; GC: Gruppo di controllo; p-Values *: Confronto tra Dn-MP e Th-MP; p-Values #: Confronto tra Dn-MP e GC; p-Values °: Confronto tra il gruppo Th-MP e GC.
DISCUSSIONE DEI RISULTATI OTTENUTI
- Abbiamo osservato un’alterazione della risposta pressoria al test dell’esercizio isometrico nei pazienti con MP di nuova diagnosi. L’esercizio isometrico valuta le vie efferenti simpatiche che innervano i vasi sanguigni attraverso l'attivazione di recettori periferici, tale risultato indica una iniziale compromissione della via simpatica vasocostrittrice nei pazienti con MP di nuova diagnosi.
- I pazienti con MP in terapia hanno mostrato un’alterata risposta pressoria al test dell’esercizio isometrico rispetto ai controlli ma non rispetto ai pazienti di nuova diagnosi, indicando che l'alterazione delle vie efferenti simpatiche vasocostrittrici nella MP tende a rimanere stabile nel tempo. Hanno invece mostrato un’alterazione delle risposte dell’arco riflesso barocettoriale al Tilt test e alla manovra di Valsalva, dimostrando una progressione e maggiore compromissione della funzione vegetativa cardiovascolare nelle fasi più avanzate di malattia.
- Non è stata rilevata una differenza significativa della funzione sudomotoria studiata tramite il Sudoscan nei pazienti di nuova diagnosi, ma invece è stata evidenziata nei pazienti con una maggiore durata e gravità di malattia. Poiché il Sudoscan è uno strumento sensibile per rilevare la neuropatia delle piccole fibre, ipotizziamo che il disturbo della sudorazione nel nostro gruppo di nuova diagnosi dipenda principalmente da un meccanismo centrale. D'altra parte, è stato dimostrato, mediante biopsie cutanee, che la patologia delle piccole fibre si verifica già nelle prime fasi della MP, quindi in alternativa il Sudoscan potrebbe avere una bassa sensibilità nel rilevare il coinvolgimento delle piccole fibre in questo stadio della malattia, mentre sembrerebbe che ci sia un coinvolgimento maggiore delle piccole fibre nervose nelle fasi più avanzate di malattia.
- Il risultato della scala di valutazione clinica SCOPA-Aut indica che i pazienti con MP di nuova diagnosi lamentano una grande varietà di sintomi vegetativi. Tuttavia, i sintomi vegetativi sono più gravi nel gruppo di pazienti in terapia suggerendo un peggioramento di tali sintomi con l’aumento della gravità e durata di malattia.
LE NOSTRE CONCLUSIONI
- Sebbene i pazienti con MP di nuova diagnosi lamentino disturbi della termoregolazione, non abbiamo riscontrato alterazioni nella funzione sudomotoria studiata tramite il Sudoscan dovuta a un possibile coinvolgimento del Sistema Nervoso Vegetativo a livello centrale.
- Il deficit della risposta vasocostrittrice simpatica all’esercizio isometrico nei MP de novo suggerisce un precoce coinvolgimento della funzione vegetativa cardiovascolare nelle fasi inziali di malattia.
BIBLIOGRAFIA
- Asahina, M., Mathias, C. J., Katagiri, A., Low, D. A., Vichayanrat, E., Fujinuma, Y., Yamanaka, Y., & Kuwabara, S. (2014). Sudomotor and cardiovascular dysfunction in patients with early untreated Parkinson's disease. Journal of Parkinson's disease, 4(3), 385–393. https://doi.org/10.3233/JPD-130326
- Bonuccelli, U., Lucetti, C., Del Dotto, P., Ceravolo, R., Gambaccini, G., Bernardini, S., Rossi, G., & Piaggesi, A. (2003). Orthostatic hypotension in de novo Parkinson disease. Archives of neurology, 60(10),1400–1404. https://doi.org/10.1001/archneur.60.10.1400
- Braune HJ,Korchounov AM, Schipper HI (1997) Autonomic dysfunction in Parkinson’s disease assessed by sympathetic skin response: a prospective clinical and neurophysiological trial on 50 patients.Acta Neurol Scand 95:293–297
- Choi BO, Bang OY, Sohn YH, Sunwoo IN (1998) Sympathetic skin response and cardiovascular autonomic function tests in Parkinson’s disease. Yonsei Med J 39:439–445.
- Goldstein D. S. (2006). Orthostatic hypotension as an early finding in Parkinson's disease. Clinical autonomic research : official journal of the Clinical Autonomic Research Society, 16(1), 46–54. https://doi.org/10.1007/s10286-006-0317-8
- Haapaniemi TH,Korpelainen JT, Tolonen U, Suominen K, Sotaniemi KA,Myllyla VV (2000) Suppressed sympathetic skin response in Parkinson disease. Clin Auton Res 10:337–342.
- Hirayama M. (2006). Sweating dysfunctions in Parkinson's disease. Journal of neurology, 253 Suppl 7, VII42–VII47. https://doi.org/10.1007/s00415-006-7010-7
- Iodice, V., Lipp, A., Ahlskog, J. E., Sandroni, P., Fealey, R. D., Parisi, J. E., Matsumoto, J. Y., Benarroch, E. E., Kimpinski, K., Singer, W., Gehrking, T. L., Gehrking, J. A., Sletten, D. M., Schmeichel, A. M., Bower, J. H., Gilman, S., Figueroa, J., & Low, P. A. (2012). Autopsy confirmed multiple system atrophy cases: Mayo experience and role of autonomic function tests. Journal of neurology, neurosurgery, and psychiatry, 83(4), 453–459. https://doi.org/10.1136/jnnp-2011-301068
- Kihara M,Kihara Y, Tukamoto T, Nishimura Y,Watanabe H,Hanakago R, Takahashi A (1993) Assessment of sudomotor dysfunction in early Parkinson’s disease. Eur Neurol 33:363–365.
- Magerkurth, C., Schnitzer, R., & Braune, S. (2005). Symptoms of autonomic failure in Parkinson's disease: prevalence and impact on daily life. Clinical autonomic research : official journal of the Clinical Autonomic Research Society, 15(2), 76–82. https://doi.org/10.1007/s10286-005-0253-z
- Maiti, P., Manna, J., & Dunbar, G. L. (2017). Current understanding of the molecular mechanisms in Parkinson's disease: targets for potential treatments. Translational neurodegeneration, 6(1), 28.
- Mano Y,Nakamuro T, Takayanagi T, Mayer RF (1994) Sweat function in Parkinson’s disease. J Neurol 241:573–576.
- Mathias, DA Low,V. Iodice, R. Bannister , Investigation of autonomic disorders, in: C J Mathias, RBannister (Eds.), Autonomic Failure: A Text Book of Clinical Disorders of the Autonomic Nervous System, 5th ed., Oxford University Press, Oxford, 2013, pp.259–287.
- Mollenhauer, B., Trautmann, E., Sixel-Döring, F., Wicke, T., Ebentheuer, J., Schaumburg, M., ... & Klein, C. (2013). Nonmotor and diagnostic findings in subjects with de novo Parkinson disease of the DeNoPa cohort. Neurology, 81(14), 1226-1234.
- Nolano, M., Provitera, V., Manganelli, F., Iodice, R., Stancanelli, A., Caporaso, G., Saltalamacchia, A., Califano, F., Lanzillo, B., Picillo, M., Barone, P., & Santoro, L. (2017). Loss of cutaneous large and small fibers in naive and l-dopa-treated PD patients. Neurology, 89(8), 776–784. https://doi.org/10.1212/WNL.0000000000004274
- Popescu C. (2019). Small fiber neuropathy in Parkinson's disease explored by the sudoscan. Parkinsonism & related disorders, 66, 261–263. https://doi.org/10.1016/j.parkreldis.2019.07.034
- Popescu C. (2020). Is sudoscan a reliable tool in detecting small fiber neuropathy in Parkinson's disease patients?. Neurodegenerative disease management, 10(2), 81–93. https://doi.org/10.2217/nmt-2019-0026
- Sasaki I, Takeuchi H, Deguchi K, Yamada A,Nishioka M, Sakamoto H(1994) Autonomic nervous function in progressive supranuclear palsy – comparison with Parkinson’s disease and healthy controls. Rinsho Shinkeigaku 34:975–979.
- Schestatsky, P., Ehlers, J. A., Rieder, C. R., & Gomes, I. (2006). Evaluation of sympathetic skin response in Parkinson's disease. Parkinsonism & related disorders, 12(8), 486–491. https://doi.org/10.1016/j.parkreldis.2006.05.029
- Siddiqui, M. F., Rast, S., Lynn, M. J., Auchus, A. P., & Pfeiffer, R. F. (2002). Autonomic dysfunction in Parkinson's disease: a comprehensive symptom survey. Parkinsonism & related disorders, 8(4), 277–284. https://doi.org/10.1016/s1353-8020(01)00052-9
- Tolosa, E., Compta, Y., & Gaig, C. (2007). The premotor phase of Parkinson's disease. Parkinsonism & related disorders, 13 Suppl, S2–S7. https://doi.org/10.1016/j.parkreldis.2007.06.007
- Visser M, Marinus J, Stiggelbout AM, Van Hilten JJ. Assessment ofautonomic dysfunction in Parkinson’s disease: the SCOPA-AUT. Mov Disord 2004;19:1306–12.
- Wüllner, U., Schmitz-Hübsch, T., Antony, G., Fimmers, R., Spottke, A., Oertel, W. H., Deuschl, G., Klockgether, T., Eggert, K., & KNP e.V (2007). Autonomic dysfunction in 3414 Parkinson's disease patients enrolled in the German Network on Parkinson's disease (KNP e.V.): the effect of ageing. European journal of neurology, 14(12), 1405–1408. https://doi.org/10.1111/j.1468-1331.2007.01982.x
- Xu X, Liao J, Dong Q, Qin F, Li J, Sun X, Lu T, Fang L, Peng F, Lu Z, Qiu W. Clinical utility of SUDOSCAN in predicting autonomic neuropathy in patients with Parkinson's disease. Parkinsonism Relat Disord. 2019 Jul;64:60-65. doi: 10.1016/j.parkreldis.2019.03.007. Epub 2019 Mar 15. PMID: 30890381.
- Zakrzewska-Pniewska B, Jamrozik Z (2003) Are electrophysiological autonomic tests useful in the assessment of dysautonomia in Parkinson’s disease? Parkinsonism Relat Disord 9:179–183.




